| F8 |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| Список кодів PDB | | 1CFG, 1D7P, 1IQD, 2R7E, 3CDZ, 3HNB, 3HNY, 3HOB, 4BDV, 1FAC, 3J2Q, 3J2S, 4KI5, 4PT6, 4XZU | | |
| Ідентифікатори |
|---|
| Символи | F8, AHF, DXS1253E, F8B, F8C, FVIII, HEMA, coagulation factor VIII, THPH13 |
|---|
| Зовнішні ІД | OMIM: 300841 MGI: 88383 HomoloGene: 49153 GeneCards: F8 |
|---|
| |
| Пов'язані генетичні захворювання |
|---|
| Васкуліт[1] |
| Онтологія гена |
|---|
| Молекулярна функція | • зв'язування з іоном металу
• GO:0001948, GO:0016582 protein binding
• oxidoreductase activity
• copper ion binding
|
|---|
| Клітинна компонента | • endoplasmic reticulum lumen
• клітинна мембрана
• extracellular region
• COPII-coated ER to Golgi transport vesicle
• endoplasmic reticulum-Golgi intermediate compartment membrane
• platelet alpha granule lumen
• Golgi membrane
• міжклітинний простір
|
|---|
| Біологічний процес | • гемостаз
• platelet degranulation
• зсідання крові
• endoplasmic reticulum to Golgi vesicle-mediated transport
• COPII vesicle coating
• acute-phase response
• blood coagulation, intrinsic pathway
• platelet activation
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
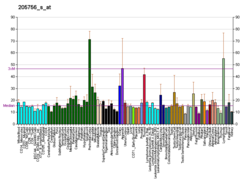 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | | NM_001161373
NM_001161374
NM_007977 |
|
|---|
| RefSeq (білок) | | | NP_001154845
NP_001154846
NP_032003 |
|
|---|
| Локус (UCSC) | Хр. X: 154.84 – 155.03 Mb | Хр. X: 74.22 – 74.43 Mb |
|---|
| PubMed search | [2] | [3] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
F8 (англ. Coagulation factor VIII, антигемофільний глобулін, АГГ, англ. AHF) — білок, який кодується однойменним геном, розташованим у людей на короткому плечі X-хромосоми.[4] Довжина поліпептидного ланцюга білка становить 2 351 амінокислот, а молекулярна маса — 267 009[5].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MQIELSTCFF | | LCLLRFCFSA | | TRRYYLGAVE | | LSWDYMQSDL | | GELPVDARFP |
| PRVPKSFPFN | | TSVVYKKTLF | | VEFTDHLFNI | | AKPRPPWMGL | | LGPTIQAEVY |
| DTVVITLKNM | | ASHPVSLHAV | | GVSYWKASEG | | AEYDDQTSQR | | EKEDDKVFPG |
| GSHTYVWQVL | | KENGPMASDP | | LCLTYSYLSH | | VDLVKDLNSG | | LIGALLVCRE |
| GSLAKEKTQT | | LHKFILLFAV | | FDEGKSWHSE | | TKNSLMQDRD | | AASARAWPKM |
| HTVNGYVNRS | | LPGLIGCHRK | | SVYWHVIGMG | | TTPEVHSIFL | | EGHTFLVRNH |
| RQASLEISPI | | TFLTAQTLLM | | DLGQFLLFCH | | ISSHQHDGME | | AYVKVDSCPE |
| EPQLRMKNNE | | EAEDYDDDLT | | DSEMDVVRFD | | DDNSPSFIQI | | RSVAKKHPKT |
| WVHYIAAEEE | | DWDYAPLVLA | | PDDRSYKSQY | | LNNGPQRIGR | | KYKKVRFMAY |
| TDETFKTREA | | IQHESGILGP | | LLYGEVGDTL | | LIIFKNQASR | | PYNIYPHGIT |
| DVRPLYSRRL | | PKGVKHLKDF | | PILPGEIFKY | | KWTVTVEDGP | | TKSDPRCLTR |
| YYSSFVNMER | | DLASGLIGPL | | LICYKESVDQ | | RGNQIMSDKR | | NVILFSVFDE |
| NRSWYLTENI | | QRFLPNPAGV | | QLEDPEFQAS | | NIMHSINGYV | | FDSLQLSVCL |
| HEVAYWYILS | | IGAQTDFLSV | | FFSGYTFKHK | | MVYEDTLTLF | | PFSGETVFMS |
| MENPGLWILG | | CHNSDFRNRG | | MTALLKVSSC | | DKNTGDYYED | | SYEDISAYLL |
| SKNNAIEPRS | | FSQNSRHPST | | RQKQFNATTI | | PENDIEKTDP | | WFAHRTPMPK |
| IQNVSSSDLL | | MLLRQSPTPH | | GLSLSDLQEA | | KYETFSDDPS | | PGAIDSNNSL |
| SEMTHFRPQL | | HHSGDMVFTP | | ESGLQLRLNE | | KLGTTAATEL | | KKLDFKVSST |
| SNNLISTIPS | | DNLAAGTDNT | | SSLGPPSMPV | | HYDSQLDTTL | | FGKKSSPLTE |
| SGGPLSLSEE | | NNDSKLLESG | | LMNSQESSWG | | KNVSSTESGR | | LFKGKRAHGP |
| ALLTKDNALF | | KVSISLLKTN | | KTSNNSATNR | | KTHIDGPSLL | | IENSPSVWQN |
| ILESDTEFKK | | VTPLIHDRML | | MDKNATALRL | | NHMSNKTTSS | | KNMEMVQQKK |
| EGPIPPDAQN | | PDMSFFKMLF | | LPESARWIQR | | THGKNSLNSG | | QGPSPKQLVS |
| LGPEKSVEGQ | | NFLSEKNKVV | | VGKGEFTKDV | | GLKEMVFPSS | | RNLFLTNLDN |
| LHENNTHNQE | | KKIQEEIEKK | | ETLIQENVVL | | PQIHTVTGTK | | NFMKNLFLLS |
| TRQNVEGSYD | | GAYAPVLQDF | | RSLNDSTNRT | | KKHTAHFSKK | | GEEENLEGLG |
| NQTKQIVEKY | | ACTTRISPNT | | SQQNFVTQRS | | KRALKQFRLP | | LEETELEKRI |
| IVDDTSTQWS | | KNMKHLTPST | | LTQIDYNEKE | | KGAITQSPLS | | DCLTRSHSIP |
| QANRSPLPIA | | KVSSFPSIRP | | IYLTRVLFQD | | NSSHLPAASY | | RKKDSGVQES |
| SHFLQGAKKN | | NLSLAILTLE | | MTGDQREVGS | | LGTSATNSVT | | YKKVENTVLP |
| KPDLPKTSGK | | VELLPKVHIY | | QKDLFPTETS | | NGSPGHLDLV | | EGSLLQGTEG |
| AIKWNEANRP | | GKVPFLRVAT | | ESSAKTPSKL | | LDPLAWDNHY | | GTQIPKEEWK |
| SQEKSPEKTA | | FKKKDTILSL | | NACESNHAIA | | AINEGQNKPE | | IEVTWAKQGR |
| TERLCSQNPP | | VLKRHQREIT | | RTTLQSDQEE | | IDYDDTISVE | | MKKEDFDIYD |
| EDENQSPRSF | | QKKTRHYFIA | | AVERLWDYGM | | SSSPHVLRNR | | AQSGSVPQFK |
| KVVFQEFTDG | | SFTQPLYRGE | | LNEHLGLLGP | | YIRAEVEDNI | | MVTFRNQASR |
| PYSFYSSLIS | | YEEDQRQGAE | | PRKNFVKPNE | | TKTYFWKVQH | | HMAPTKDEFD |
| CKAWAYFSDV | | DLEKDVHSGL | | IGPLLVCHTN | | TLNPAHGRQV | | TVQEFALFFT |
| IFDETKSWYF | | TENMERNCRA | | PCNIQMEDPT | | FKENYRFHAI | | NGYIMDTLPG |
| LVMAQDQRIR | | WYLLSMGSNE | | NIHSIHFSGH | | VFTVRKKEEY | | KMALYNLYPG |
| VFETVEMLPS | | KAGIWRVECL | | IGEHLHAGMS | | TLFLVYSNKC | | QTPLGMASGH |
| IRDFQITASG | | QYGQWAPKLA | | RLHYSGSINA | | WSTKEPFSWI | | KVDLLAPMII |
| HGIKTQGARQ | | KFSSLYISQF | | IIMYSLDGKK | | WQTYRGNSTG | | TLMVFFGNVD |
| SSGIKHNIFN | | PPIIARYIRL | | HPTHYSIRST | | LRMELMGCDL | | NSCSMPLGME |
| SKAISDAQIT | | ASSYFTNMFA | | TWSPSKARLH | | LQGRSNAWRP | | QVNNPKEWLQ |
| VDFQKTMKVT | | GVTTQGVKSL | | LTSMYVKEFL | | ISSSQDGHQW | | TLFFQNGKVK |
| VFQGNQDSFT | | PVVNSLDPPL | | LTRYLRIHPQ | | SWVHQIALRM | | EVLGCEAQDL |
| Y |
Задіяний у таких біологічних процесах, як зсідання крові, гемостаз, гостра фаза запалення, альтернативний сплайсинг. Білок має сайт для зв'язування з іонами металів, іоном кальцію. Секретований назовні.
Історія
VIII-фактор вперше було відкрито в 1937 році, але аж 1979 році Едвардо Тудденхем[en] та його співробітники зуміли очистити білок, що дозволило здійснити молекулярну ідентифікацію білка[6].
Препарати
На основі фактору згортання крові VIII створений препарат під назвою Мороктоког альфа, який застосовують під час лікування гемофілії А.[7]
Див. також
Примітки
- ↑ Захворювання, генетично пов'язані з F8 переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:3546 (англ.) . Процитовано 12 вересня 2017.
- ↑ UniProt, P00451 (англ.) . Архів оригіналу за 6 вересня 2017. Процитовано 12 вересня 2017.
- ↑ Tuddenham EG, Trabold NC, Collins JA, Hoyer LW (1979). The properties of factor VIII coagulant activity prepared by immunoadsorbent chromatography. J Lab Clin Med. 93: 40–53.
- ↑ (англ.)ReFacto AF [Архівовано 12 листопада 2020 у Wayback Machine.]
Література
- Levinson B., Kenwrick S., Gamel P., Fisher K., Gitschier J. (1992). Evidence for a third transcript from the human factor VIII gene. Genomics. 14: 585—589. PMID 1427887 DOI:10.1016/S0888-7543(05)80155-7
- Gitschier J., Wood W.I. (1992). Sequence of the exon-containing regions of the human factor VIII gene. Hum. Mol. Genet. 1: 199—200. PMID 1303178 DOI:10.1093/hmg/1.3.199
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Severs J.C., Carnine M., Eguizabal H., Mock K.K. (1999). Characterization of tyrosine sulfate residues in antihemophilic recombinant factor VIII by liquid chromatography electrospray ionization tandem mass spectrometry and amino acid analysis. Rapid Commun. Mass Spectrom. 13: 1016—1023. PMID 10368977 DOI:10.1002/(SICI)1097-0231(19990615)13:11<1016::AID-RCM599>3.0.CO;2-5
- Pittman D.D., Wang J.H., Kaufman R.J. (1992). Identification and functional importance of tyrosine sulfate residues within recombinant factor VIII. Biochemistry. 31: 3315—3325. PMID 1554716 DOI:10.1021/bi00128a003
- Saenko E.L., Scandella D. (1997). The acidic region of the factor VIII light chain and the C2 domain together form the high affinity binding site for von Willebrand factor. J. Biol. Chem. 272: 18007—18014. PMID 9218428 DOI:10.1074/jbc.272.29.18007
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|











